特定全营养配方食品VS其他特医食品:差异解析、临床运用与配方依据
PART.1
特定全营养配方食品有哪些?和其他类型特医食品的区别是什么?
1、特殊医学用途配方食品分类
特殊医学用途配方食品根据适用人群不同分为:适用于0月龄至12月龄的特殊医学用途婴儿配方食品和适用于1岁以上人群的特殊医学用途配方食品。根据患有特殊紊乱、疾病或医疗状况婴儿的特殊营养需求,《食品安全国家标准 特殊医学用途婴儿配方食品通则》(GB25596-2010)中列出了6种常见的特殊医学用途婴儿配方食品(见图1)。[1-3]根据不同临床需求和适用人群,《特殊医学用途配方食品通则》(GB29922-2013)将该类产品分为以下三类:
· 全营养配方食品:适用于需对营养素进行全面补充且对特定营养素没有特别要求的人群。
· 特定全营养配方食品:适用于特定疾病或医学状况下需对营养素进行全面补充的人群,并可满足人群对部分营养素的特殊需求。
· 非全营养配方食品:适用于需要补充单一或部分营养素的人群。

(图片摘自文献[3]”特殊医学用途配方食品和药品注册要求比较分析”)
2、13种特定全营养配方食品
GB29922-2013将特定全营养配方食品分为13种:①糖尿病全营养配方食品,②呼吸系统疾病全营养配方食品,③肾病全营养配方食品,④肿瘤全营养配方食品,⑤肝病全营养配方食品,⑥肌肉衰减综合征全营养配方食品,⑦创伤、感染、手术及其他应激状态全营养配方食品,⑧炎性肠病全营养配方食品,⑨食物蛋白过敏全营养配方食品,⑩难治性癫痫全营养配方食品,⑪胃肠道吸收障碍、胰腺炎全营养配方食品,⑫脂肪酸代谢异常全营养配方食品,⑬肥胖、减脂手术全营养配方食品。[1-3]
值得一提的是,在2022年12月,中国疾病预防控制中心营养与健康所和国家食品安全风险评估中心共同制定的《食品安全国家标准 特殊医学用途配方食品通则》(草案)中,将13种调整成了12种(如下图),变更食物蛋白过敏全营养配方食品、难治性癫痫全营养配方食品为部分营养调整型全营养配方类别,新增了1个其他类别。由于该通则为草案,本文将延续GB29922-2013的13种分类。

(图片摘自文献[9]“《食品安全国家标准 特殊医学用途配方食品通则》(草案)”)
3、特定全营养配方食品和其他类型特医食品的区别是什么?
(1)能适应不同疾病的特异性代谢状态
特定全营养配方食品是在相应年龄段全营养配方食品的基础上,依据特定疾病的病理生理变化而对部分营养素进行适当调整的一类食品,单独食用时即可满足目标人群的营养需求。符合特定全营养配方食品技术要求的产品,可有针对性的适应不同疾病的特异性代谢状态,更好地起到营养支持作用。[2]
(2)较其他特医食品监管更加严格
2023年6月15日颁布的《食品经营许可和备案管理办法》(市场监管总局令第78号),对销售特殊医学用途配方食品中的特定全营养配方食品明确了新要求:“特定全营养配方食品较其他特医食品监管更加严格。”[4-5]具体表现为以下几点:
· 企业申请特定全营养配方食品产品注册前必须完成不少于100例病人的临床试验;
· 国家对包括特定全营养配方食品的特医食品实施产品注册管理;
· 各地方市场监管局对企业实施生产许可管理,企业取得生产许可证后方可生产;
· 特定全营养配方食品广告要求按照处方药广告管理,其他类别的特医食品广告按非处方药广告管理;
· 特定全营养配方食品只能通过医疗机构或者药店零售企业向消费者销售,不能进行网络销售;
· 医疗机构、药店零售企业销售特定全营养配方食品的,不需要取得食品经营许可或备案,但应当遵守《食品安全法》及其实施条例关于食品销售的规定;
· 这次《食品经营许可和备案管理办法》又新增规定,向医疗机构、药品零售企业销售特定全营养配方食品的经营企业,应当取得食品经营许可或者进行备案。
PART.2
特定全营养配方食品的临床运用现状如何?
1、目前特定全营养配方食品无法满足临床需求
李雪梅等[7]在2023年10月发表了文章《全国592家医疗机构肠内营养制剂的临床供给、应用及需求调查》,研究了592家二级及以上综合或专科医院的肠内营养制剂应用现状。研究结论如下:
(1)FSMP整体市场占有率低,三者共存局面或将持续
目前院内肠内营养制剂仍以肠内营养药品为主,获批的FSMP主要为进口和婴幼儿产品,粉状成品使用率最高,61.5%的医院仍使用未获得FSMP注册批号的固体/液体饮料。肠内营养药品、FSMP、固体/液体饮料三者共存局面或将持续。研究分析造成目前三者并存局面的可能原因有:①肠内营养药品上市较早,临床已形成使用习惯,且能进入医保报销,减轻患者医疗负担;②目前获批FSMP产品种类以婴幼儿配方为主,使用较为局限,而成人产品数量相对较少;③目前获批FSMP产品以进口为主,由于开发成本高,审批时间长,导致价格奇高,在很大程度上限制了其在临床的使用;④开具FSMP的主要为临床营养师,而临床营养学科发展滞后,其临床应用自然有限,而医护人员对FSMP不甚了解,仍延续开药的习惯;⑤目前正处于FSMP发展过渡期,为了满足临床需求,行政上并未完全限制医疗机构使用固体/液体饮料。[7]
(2)亟需加快成人型特定全营养配方食品上市
此次调查显示,341家(57.6%)表示,现有肠内营养制剂不能够满足临床需求。尤其是肿瘤、肾病、糖尿病、创伤/感染/手术及其他应激状态,胃肠道吸收障碍/胰腺炎等疾病专用配方,然而71.8%的医院拥有的药字号肠内营养产品不超过5种,无法满足所有临床需求。[7]
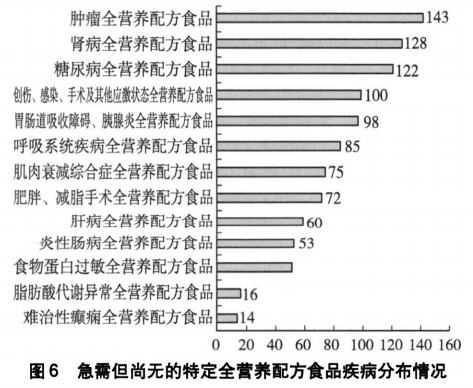
(图片摘自文献[7]“全国592家医疗机构肠内营养制剂的临床供给、应用及需求调查”)
研究者分析认为,尽管国家从政策上大力发展FSMP产业,不再批准新的肠内营养药品上市,但目前仅有一款获批的特定疾病全营养配方产品(肿瘤型,详见下文),使很多医院只能继续使用产品安全性和效果均无法保障的固体/液体饮料。364家有固体/液体饮料的医院中,有80.2%的医院在使用类似特定全营养配方食品的固体或液体饮料。因此,企业需加快特定全营养配方食品的研发、临床试验,相关政府职能部门应加快其审批速度,促其尽快入市以满足临床需求。[7]
2、我国截止目前仅批准了一款特定全营养配方食品
截至目前(2023年11月),市场监管总局批准了一款特定全营养配方食品,即特殊医学用途肿瘤全营养配方食品[5],其具体信息可到国家市场监督管理总局特殊食品信息查询平台查询。该产品的适用人群是10岁以上存在营养风险或营养不良的肿瘤患者。
PART.3
特定全营养配方食品设计的配方依据和技术要求是什么?
前面提到“特定全营养配方食品是在相应年龄段全营养配方食品的基础上,依据特定疾病的病理生理变化而对部分营养素进行适当调整的一类食品”,那么国家对于不同类型特定全营养配方食品设计的具体配方依据和技术要求是什么呢?
在“《特殊医学用途配方食品通则》(GB 29922-2013)问答”[2]中,对8种科学证据充分、应用历史长的特定全营养配方食品明确了其在全营养配方食品基础上可调整的营养素含量技术指标。其他5种特定全营养配方食品由于目前营养素调整证据尚不充分,该问答暂未规定其营养素调整范围,同时也表示“今后将随着科学证据的不断积累,根据临床营养支持需要,在充分保证其安全性和科学性的前提下,通过修改问答的方式完善其技术指标。”接下来一起了解下GB 29922-2013问答对8种特定全营养配方食品的要求吧!

(1)糖尿病病人用全营养配方食品
糖尿病患者由于遗传因素、内分泌功能紊乱等原因引发糖、蛋白质、脂肪、水和电解质等一系列代谢紊乱。针对上述情况,该类产品调整了宏量营养素的比例和钠的含量,强调产品的低血糖生成指数(低GI),为患者提供全面而均衡的营养支持。
糖尿病病人用全营养配方食品应满足如下技术要求:
1)应为低GI配方,GI≤55。
2)饱和脂肪酸的供能比应不超过10%。
3)碳水化合物供能比应为30-60%,膳食纤维的含量应不低于0.3g/100kJ(1.4g/100kcal)。
4)钠的含量应不低于7mg/100kJ(30mg/100kcal),不高于42mg/100kJ(175 mg/100kcal)。
(2)COPD病人用全营养配方食品
慢性阻塞性肺疾病(COPD)是呼吸系统疾病中的一种。为了减少肺部二氧化碳潴留,COPD患者需要适当的营养支持,并需要适量添加中链甘油三酯(MCT)以减轻胃肠负担,同时可在配方中选择性添加n-3脂肪酸。
COPD病人用全营养配方食品应满足如下技术要求:
1)脂肪供能比应为30%-55%;当脂肪供能比>40%时,中链甘油三酯(MCT)提供的能量应为总能量的10%-20%。
2)如果添加n-3脂肪酸(以EPA和DHA计),在配方中的供能比应为1%-6%,同时对亚油酸和α-亚麻酸的供能比不再做相应要求。
(3)肾病病人用全营养配方食品
肾病病人用全营养配方食品适用于成人慢性肾脏病(CKD)患者,配方根据透析或非透析慢性肾脏病患者对营养素的不同需求,通过调整蛋白质及电解质的水平,以满足其营养需要。
1)对于非透析慢性肾脏病患者,产品配方具体技术要求如下:
配方中蛋白质含量应不高于0.65g/100kJ(2.7g/100kcal),其他营养素应调整的范围如表1。
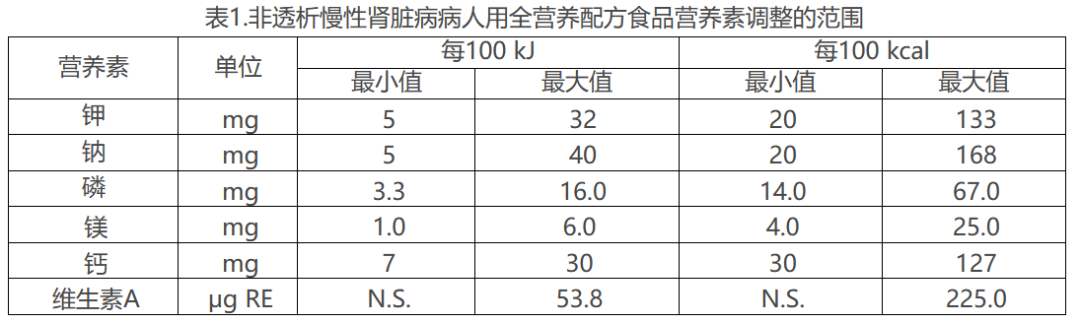
2)对于透析治疗的患者,产品配方具体技术要求如下:
配方中蛋白质含量应不低于0.8g/100kJ(3.3g/100kcal),其他营养素应调整的范围如表2。
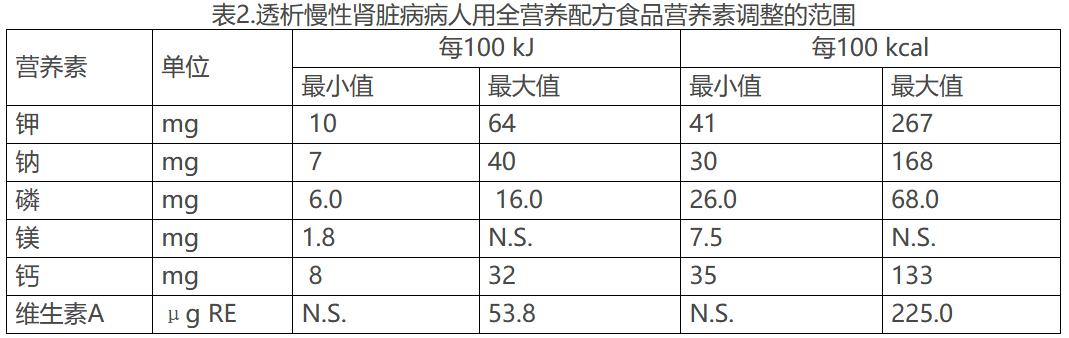
(4)恶性肿瘤(恶病质状态)病人用全营养配方食品
手术期、恶液质期的恶性肿瘤(恶病质状态)患者由于肿瘤的消耗、阻碍进食和消化、以及肿瘤对食欲的影响、患者精神抑郁等因素,伴随的以体重下降为特征的营养不良比较常见,因此应尽早对患者进行营养补充。
该特定全营养配方产品应适当提高蛋白质的含量并调整与机体免疫功能相关的营养素含量,为患者提供每日所需的营养物质。
恶性肿瘤(恶病质状态)病人用全营养配方食品应满足如下技术要求:
1)蛋白质的含量应不低于0.8 g/100kJ (3.3 g/100kcal)。
2)n-3脂肪酸(以EPA和DHA计)在配方中的供能比应为1%-6%,同时对亚油酸和α-亚麻酸的供能比不再做相应要求。
3)可选择添加营养素(精氨酸、谷氨酰胺、亮氨酸)。如果添加精氨酸,其在产品中的含量应不低于0.12g/100 kJ (0.5g/100kcal);如果添加谷氨酰胺,其在产品中的含量应为0.04g/100kJ -0.53g/100kJ(0.15g/100kcal- 2.22g/100kcal);如果添加亮氨酸,其含量应不低于0.03g/100kJ(0.13g/100kcal)。
(5)炎性肠病病人用全营养配方食品
炎性肠病主要包括溃疡性结肠炎(UC)和克罗恩病(CD)。UC和CD均为肠道非特异性疾病。由于病变主要发生在消化道,既妨碍营养物质的摄入、消化和吸收,又造成营养物质从肠道不同程度的丢失。针对上述情况,配方应使用易消化吸收的蛋白质和脂肪来源,以改善患者的营养状况和临床症状。
炎性肠病病人用全营养配方食品应满足如下技术要求:
1) 可以选用整蛋白、食物蛋白质水解物、肽类和/或氨基酸作为蛋白质的来源;
2)脂肪供能比应不超过40%,其中中链甘油三酯(MCT)含量应不低于总脂肪的40%。
(6)食物蛋白过敏病人用全营养配方食品
该类配方食品作为《特殊医学用途婴儿配方食品通则》(GB 25596-2010)中适用于食物蛋白过敏婴儿的配方食品的一个延续,适用于1岁以上的食物蛋白过敏患者。
此类食品的配方应为食物蛋白深度水解配方或氨基酸配方,即采用一定的工艺将引起过敏反应的食物蛋白水解成短肽和游离氨基酸,或者直接采用单体氨基酸代替蛋白质。所使用的氨基酸来源应符合本标准附录B或《食品营养强化剂使用标准》(GB 14880-2012)的规定。
(7)难治性癫痫病人用全营养配方食品
生酮饮食是难治性癫痫病人的主要营养支持途径。该类全营养配方食品采用高脂肪、低碳水化合物和适量蛋白质的配方(即生酮饮食配方),在提供营养的同时为大脑提供必要的能量,缓解癫痫的发作。
难治性癫痫病人用全营养配方食品中脂肪与(蛋白质+碳水化合物)的质量比范围应在1:1-5:1之间。
(8)肥胖、减脂手术病人用全营养配方食品
肥胖、减脂手术病人由于代谢紊乱而导致蛋白质和微量营养素摄入不足现象,该类特定全营养配方食品的配方特点为在提供较低能量的同时可以保证充足的蛋白质和微量营养素(维生素、矿物质等)的供应,适用于肥胖、减脂手术病人。其产品配方应满足如下技术要求:
1)根据产品使用说明,每日摄入的能量为600-1200kcal;
2)为保证蛋白质和微量营养素的摄入,每100 kcal产品中应适当增加某些营养素的含量,调整范围如表3。

PART.4
结 语
由李雪梅等[7]对肠内营养制剂临床应用现状调查可知,目前肠内营养药品、FSMP和固体/液体饮料三者同存,在一定程度上满足了临床需求,但从长远来看不利于FSMP产业发展和医疗机构监管。有关部门应加强FSMP标准制定和市场规范,尽快出台政策引导产业向成人、疾病专用型、组件类别产品研发和布局,逐步从三足鼎立过渡到FSMP全面覆盖。
2022年1月,国家卫健委在官网就代表们提出的《关于加快特殊医学用途特定全营养配方食品国家标准出台的建议》给出了答复[8]:
· 13类特定全营养配方食品已立项制定9类标准,其中糖尿病、炎性肠病、肿瘤等3项已完成起草,并公开征求意见。
· 正组织对GB 29922、GB 25596、GB 29923进行修订;并将研制《特殊医学用途配方食品临床应用指南》《中重度营养不良用营养补充食品》《结核病患者营养补充食品》《阿尔茨海默病患者营养补充食品》等相关标准。
· 将会同市场监管总局继续加快特定全营养配方食品相关的食品安全国家标准制修订工作,持续推进标准审查,加大食品安全监管力度。
以上答复也在后续工作得到体现,如2022年12月,中国疾病预防控制中心营养与健康所和国家食品安全风险评估中心共同承担完成了《食品安全国家标准 特殊医学用途配方食品通则》(草案);2023年8月市场监管总局特殊食品司发布了《特殊医学用途配方食品临床试验质量管理规范(征求意见稿)》;2023年10月,食品安全标准与监测评估司发布了《食品安全国家标准肿瘤全营养配方食品(征求意见稿)》等等。
此外,关于FSMP的临床规范应用,临床营养学科领域也发布了《特殊医学用途配方食品(FSMP)临床管理专家共识(2021版)》、《肿瘤患者特殊医学用途配方食品使用指南(2022版)》等指南共识。
可以期待相关政府部门政策标准的进一步完善,医院内PSMP规范应用的推广,以及特医企业自主研发和供应等多方面的合作,共同推动FSMP的规范应用,最终让患者受益!

素材来源网络,如侵删
- 三项特医食品特定全营养配方... 2026-05-20
- 近日,国家卫生健康委员会正式发布三项特殊医学用途配方食品特定全营养配方食品安全国家标准征求意见稿,涉及糖尿病全营养配方食品、肥胖症及...【详细】

