肿瘤患者食欲下降的营养诊疗专家共识
由于肿瘤本身及手术、放化疗等治疗因素影响, 肿瘤患者常出现食欲下降。 食欲下降导致的营养摄入不足易引起营养不良和恶液质, 可使肿瘤患者对抗肿瘤治疗的耐受性及疗效降低、生活质量下降, 严重影响患者生存预后。 在病程中准确评估患者食欲, 结合营养筛查与评估, 尽早发现患者营养风险并给予个体化的营养治疗, 有利于改善患者食欲与营养状况、预防或延缓病程进展、提高治疗耐受性, 对于改善患者的预后及生活质量具有积极意义。 为规范肿瘤患者食欲下降的营养诊疗, 提高救治效果, 本共识根据国内外现有研究成果, 综合有关专家意见和临床经验, 阐述了肿瘤患者食欲下降的定义与发生机制, 提供了厌食 / 恶液质评价量表、肿瘤患者食欲症状问卷、食欲刻度尺等食欲评价工具, 并且给出了肿瘤患者食欲下降的营养治疗建议。 希望本共识的发布可以提高临床医护人员及临床营养(医)师对于肿瘤患者食欲下降的识别、评估和营养治疗水平, 使患者临床获益。
背 景
根据国际癌症研究机构发布的最新统计数据显示, 2020年全球新发恶性肿瘤病例数 1930 万例, 死亡病例近 1000 万例, 其中我国恶性肿瘤的新增病例与死亡人数位居世界首位。肿瘤患者在病程进展过程中, 常因为疾病本身与抗肿瘤治疗导致食欲下降, 且其在肿瘤不同时期的发生率不同。
据统计, 厌食在新诊断的肿瘤患者中发生率约为50%, 在晚期患者中可达26. 8% ~ 57. 9% 。食欲下降导致的营养摄入不足可引起营养不良与恶液质, 导致患者对抗肿瘤治疗的耐受性及疗效下降, 进一步影响临床结局。研究显示, 有10% ~ 20%的肿瘤患者直接死亡原因为营养不良。然而, 仅有 30% ~ 60%伴营养不良的肿瘤患者接受了营养干预, 包括口服营养补充(oral nutritional supplements,ONS)、肠内营养和肠外营养。
肿瘤患者食欲下降及恶液质
食欲下降、进食障碍相关定义食欲是刺激机体摄入食物的一种主观感受, 在广义上涉及到一些生理和心理学过程, 生理因素包括进食的欲望、饥饿感、饱腹感等, 心理因素包括食物的组成及从进食中获得的乐趣。食欲下降是饥饿感减退或丧失、早饱,或主观意愿上进食部分改变或完全丧失。进食障碍是指以反常的摄食行为和心理紊乱为特征 ,伴随显著的体重改变或生理功能紊乱的一组综合征, 神经性厌食症属于进食障碍的一种。厌食症指无论体重是否减少, 患者出现食欲减退的一种病理表现。为表述方便,本共识将食欲下降、进食障碍、厌食症统一表述为食欲下降。肿瘤患者食欲下降的发生机制肿瘤相关性厌食症根据发病原因可分为原发性厌食症与继发性厌食症。原发性厌食症的原因目前尚不清楚, 研究结果显示其可能与肿瘤细胞诱导机体释放的某些活性因子相关,如白介素-1( interleukin-1,IL-1)、白介素-6( interleukin - 6,IL- 6) 及肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)。神经肽与中枢神经系统其他神经递质间神经内分泌通路的紊乱也可能导致厌食、早饱等症状 。消化道肿瘤占位还可能引起消化道梗阻, 导致腹胀和食欲下降。抑郁、便秘、疼痛和接受抗肿瘤治疗是导致继发性厌食症的常见原因。化疗药物在杀死肿瘤细胞的同时也会损伤一些正常细胞, 多种化疗药物会引起恶心、呕吐、味觉改变、腹泻、胃肠道黏膜损伤等消化道不良反应, 导致患者食欲下降。此外, 上消化道肿瘤及头颈部肿瘤放疗患者常出现口腔溃疡、疼痛、吞咽困难、味觉改变、口干, 同时伴随着食欲下降或者无食欲。研究显示,食管癌患者接受新辅助化疗期间,体重平均减轻 4. 2 kg; 头颈部肿瘤患者同步放化疗期间, 体重平均减轻11. 4 kg。厌食-恶液质综合征肿瘤患者的食欲下降不是孤立症状, 常与疼痛、疲劳、虚弱等其他症状同时出现, 但即使考虑了其他因素, 仍发现肿瘤相关性厌食症对患者的生活质量有显著影响。厌食或摄入减少是恶液质发展的主要因素,也被称为厌食-恶液质综合征 ( cancer anorexia - cachexia syndrome,CACS), 大约 50% 的肿瘤患者患有 CACS。因为肿瘤类型、分期、治疗、食物摄入、心理等方面的改变, CACS被认为是一种多因素共同作用的复杂综合征,主要表现为食欲下降,非自主的体重减轻以及骨骼肌丢失, 可直接导致患者预后不良以及生活质量下降。
肿瘤患者食欲下降的食欲评价与营养评估
肿瘤患者食欲评价准确评估患者食欲有助于医护人员尽早识别可能受益于营养治疗的肿瘤患者。但目前尚无评估肿瘤患者食欲下降的金标准,常用的评价方法包括问卷法、生物标志物法、膳食模式法等, 通常采用问卷法对其进行定量评价。肿瘤患者厌食/ 恶液质评价量表Ribaudo JM等将厌食 / 恶液质治疗功能评估量表( functionalassessment of anorexia / cachexia therapy, FAACT) 简化为12个问题, 即肿瘤患者厌食 / 恶液质评价量表(anorexia / cachexia subscale-12, A / CS-12), 用以评估厌食 / 恶液质, 并进行了有效性验证, 具体评价标准见表 1。建议总评分≤30 分即可认为患者存在食欲下降。

肿瘤患者食欲症状问卷Halliday V 等基于营养食欲问卷( council of nutrition appetite questionnaire, CNAQ) 开发了肿瘤患者食欲症状问卷(cancer appetite and symptom questionnaire, CASQ), 用以预测肿瘤患者体重丢失,为早期通过食欲情况判断患者体重下降可能提供参考。CASQ 由 12个条目组成, 总得分 0 ~ 48 分, 分数越低代表症状负担更大和 / 或食欲下降越明显 。具体评价标准见表 2。CASQ 被证实具有良好的信度与效度, 在预测肺癌和上消化道肿瘤患者体重丢失>10%时, 最佳评分截止点为 29 或 30, 但其阳性预测值和特异度较低。
。具体评价标准见表 2。CASQ 被证实具有良好的信度与效度, 在预测肺癌和上消化道肿瘤患者体重丢失>10%时, 最佳评分截止点为 29 或 30, 但其阳性预测值和特异度较低。
口腔评价工具表针对头颈部肿瘤放疗患者, 日本学者提出了针对口腔问题的食欲评价工具表, 分为 3 部分进行评估, 共计 14 项, 每项满分为 5 分(1 分= 完全不,5 分 = 非常), 分数越高代表食欲越差。分析结果显示具有较好的信度和效度, 具体评价标准见表3。
食欲刻度尺由于传统食欲评价方法较为复杂,可采用食欲刻度尺量化患者的主观 食欲感觉。食欲刻度尺包括 0 ~ 10 级,其中 0 代表食欲最差, 10 代表食欲最好,具体评价标准见图1。

肿瘤患者营养风险筛查与评估
肿瘤患者应常规进行营养风险筛查与评估,以早期识别患者营养风险、营养不良及其严重程度,保证营养治疗的合理应用。目前推荐用于肿瘤患者营养风险筛查与评估的工具主要包括:营养风险筛查 2002( nutritional risk screening 2002, NRS 2002)、患者主观整体评估 ( patient - generated subjective global assessment, PG-SGA)。通过进一步的综合测定(应激反应、炎症反应、能耗水平、代谢状况、器官功能、人体组成成分分析、心理状况等), 甄别患者营养不良的类型与原因,进行个体化的营养治疗。肿瘤患者膳食评价工具传统方法针对肿瘤患者因食欲下降出现的摄入不足,营养(医)师通常采用 24 h 膳食回顾法、三日饮食称重法和食物频率问卷等方法评估患者的能量摄入情况。简明膳食自评工具丛明华和石汉平提出的肿瘤患者简明膳食自评工具,可用于动态评估饮食摄入情况,具体评价标准见表 4。在头颈部肿瘤与食管癌术后患者中,简明膳食自评工具表现出良好的信效度,但是该表不适用于评价所有类型的肿瘤患者及肿瘤患者在住院期间医疗膳食的摄入情况。
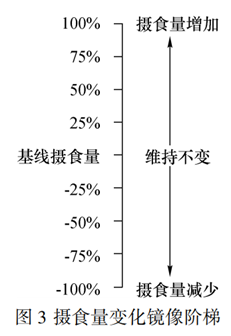
简易膳食评价摄食量刻度尺与摄食量变化镜像阶梯可用于量化摄食量与摄食情况变化。摄食量刻度尺包括 0 ~ 10 级,其中 0 代表完全没吃, 6 以上表示摄入良好,10 代表吃得最多。摄食量变化镜像阶梯以基线摄食量为 0,0 ~ 100%为摄食量增加, -100% ~0 为摄食量减少,患者可根据自己的摄食情况选择相应数字。具体评价标准见图 2、3。
肿瘤患者食欲下降的营养治疗
营养治疗原则由于肿瘤患者普遍存在食欲下降和多因素所致的营养不良, 而食欲下降对患者生活质量的负面影响与不良预后相关, 营养治疗应作为肿瘤治疗的基础手段,以解决患者食欲下降导致的摄食量不足, 维持肌肉质量和身体功能。肿瘤患者的能量需求可采用间接能量测定法或估算法计算。间接能量测定法较为准确, 但需配备间接能量测定仪,对设备和操作技术要求较高。估算法较为简便, 适用范围更加广泛。推荐给予非肥胖肿瘤患者与健康者相似的能量目标需要量, 即 25 ~ 30 kcal / ( kg· d), 并综合参考患者体温系数、应激系数和活动系数, 以满足大多数患者的能量需求。在非荷瘤状态下三大营养素的供能比为:碳水化合物 50% ~ 55%, 脂肪 25% ~ 30%, 蛋白质15% ~ 20%。在荷瘤状态下可适当减少碳水化合物的供能比。对于有营养不良风险的患者, 营养治疗应遵循阶梯原则。首先选择营养教育和饮食指导, 对于无法经口摄入足够营养者, 如消化道功能正常或具有部分消化道功能, 鼓励患者使用 ONS。当饮食+ONS不能满足 60%目标能量需求 3 ~ 5 d 时, 应该选择肠内营养。当肠内营养不能满足营养需求时, 可加用肠外营养,必要时采用全肠外营养。需要注意的是, 评估严重营养不良或持续性进食过少者, 建议缓慢增加营养补充( ONS、肠内或肠外), 并采取额外的措施以防止发生再喂养综合征。对于此类高危人群, 建议营养治疗的前 24 h 给予10 ~20 kcal / kg,每 1 ~ 2 天增加 33%目标能量,过程中需注意补充微量营养素。肿瘤患者食欲下降的干预措施肿瘤患者食欲下降的饮食调整方法针对肿瘤患者的厌食症状, 需要调整食物的色香味、质地及少量多餐的摄入模式以增强食欲,增加营养摄入, 提高患者生活质量。具体调整方法可参考表 5。

不同治疗方式食欲下降肿瘤患者的营养治疗非终末期放化疗患者:放化疗期间食欲下降的营养治疗目标是改善患者营养摄入、维持体重和体能状态、增加治疗耐受性、改善患者生活质量。治疗期间, 能量推荐摄入量为 25 ~ 30 kcal / (kg· d); 蛋白质最低摄入量为 1. 0 g / ( kg· d), 目标需要量为 1. 2 ~ 2. 0 g / (kg· d)。合并慢性肾病患者,需适当限制蛋白质摄入量[36]。当患者已有营养不良或放化疗严重影响摄食且预期持续时间大于1周者, 应进行营养治疗,如 ONS 或管饲肠内营养达不到需要量, 需结合肠外营养或全肠外营养。此外, 推荐使用 ω-3 多不饱和脂肪酸(ω-3 polyunsaturated fatty acids, ω-3PUFAs)或鱼油补充剂, 以改善放化疗肿瘤患者的食欲, 维持或增加瘦体组织与体重。非终末期手术患者:非终末期手术患者食欲下降的营养治疗目标是提高食欲,改善患者经口进食能力,减少高代谢压力下身体产生的分解反应, 促进术后创伤愈合。对于术前评估为营养不良和/ 或营养不良高风险的患者, 建议术前 1 ~ 2 周进行营养治疗,必要时延后手术时间, 并缩短禁食禁水时间, 术后尽早进食[30]。如术后经口摄食预期不能满足 60%需要量 1 周以上,应给予术后营养治疗。围手术期要保证蛋白质摄入量达标。对于需要进行腹部大手术的患者, 推荐术前 5 ~ 7 d 补充免疫增强型的 ONS , 并持续到术后 1 周或者经口摄食>60%需要量。终末期患者:因终末期肿瘤患者疾病无法逆转且营养治疗可能会导致并发症, 干预措施应该选用非侵入性的, 主要针对心理和生存进行支持。终末期肿瘤患者营养治疗的目标是减少饥饿感、提高患者生活质量。食欲下降肿瘤患者的特殊医学用途配方食品应用意见特殊医学用途配方食品(food for special medical purpose, FSMP)是指为满足进食受限、消化吸收障碍、代谢紊乱或特定疾病状态人群对营养素或者膳食的特殊需要, 专门加工配制而成的配方食品。对于无法经口摄入足够营养的肿瘤患者, 建议 ONS 补充 400 ~ 600 kcal / d。如果 ONS 不能满足需求,需考虑采用管饲肠内营养和/ 或肠外营养以补充能量。肿瘤患者的 FSMP 配方应考虑患者口味, 提供充足的能量与优质蛋白质。与均衡饮食相比, 提高脂肪比例可以提高食物能量密度, 有助于保持或增加患者体重。此外, FSMP 可选择添加适量免疫营养素, 如 ω-3PUFAs、谷氨酰胺等。ω-3PUFAs:ω-3PUFAs 中的 EPA 与 DHA有助于减缓体重丢失, 提高肿瘤化疗的耐受性,延缓恶液质的发生。ω-3PUFAs 可以降低炎症指标 IL-6 和 C 反应蛋白( c-reactive protein,CRP)水平, 可能对癌性厌食发挥一定程度的治疗作用。非对照临床研究显示, 单独使用鱼油或与其他营养补充剂联用, 可减缓胰腺癌患者体重下降。每日摄入 2 g ω-3PUFAs 或 4 ~ 6 g 鱼油有利于维持瘦体组织、改善食欲与无力感、降低化疗的神经毒性反应, 并进一步改善肿瘤患者生活质量。谷氨酰胺:谷氨酰胺对于减轻肿瘤放化疗患者黏膜损伤(口腔黏膜炎、食管炎、肠炎等),改善或维持患者生活质量具有潜在有益作用。一项纳入 15 个临床试验的系统评价发现, 补充谷氨酰胺可显著降低肿瘤患者黏膜炎发生率、严重程度与持续时间,减缓体重下降。但在另一项针对头颈部肿瘤放疗患者的 RCT 研究中, 谷氨酰胺对于口腔黏膜炎和颈部皮炎的发生率和严重程度没有明显改善。基于现有研究结果的异质性, 目前不推荐对肿瘤患者常规补充谷氨酰胺。食欲下降肿瘤患者的营养教育肿瘤患者食欲下降与肿瘤本身、抗肿瘤治疗以及焦虑、恐惧等心理问题密切相关,更加需要接受长期、可持续的营养教 育, 以 维 持 健 康 饮 食 习 惯 和 良 好 生 活 习惯。研究证实,在营养治疗中强化营养教育有利于改善肿瘤患者的体重与营养状况,提高治疗依从性。在营养教育过程中, 需让患者充分认识相关饮食误区, 了解营养对疾病康复的重要性, 养成良好饮食习惯。鼓励患者定期监测体重, 优先摄入营养密度高且患者喜爱的食物, 通过少食多餐的方式摄入足量食物, 从而改善营养与健康。食欲下降肿瘤患者的运动食欲下降的肿瘤患者, 应鼓励其通过进行身体锻炼来维持和改善食欲, 并根据健康状况和身体功能水平增减运动强度。由于运动锻炼会增加机体能量的消耗, 为避免患者减轻体重, 保持肌肉含量, 在运动干预时应同时提供充足的能量和蛋白质补充。
推荐意见
食欲下降是肿瘤患者的常见症状,易引起营养不良和恶液质, 影响肿瘤的治疗以及预后。建议常规实施食欲评价、营养筛查与营养评估, 尽早发现患者营养风险并给予营养治疗(A, 强推荐)。对于存在营养不良或营养不良高风险的放化疗及围手术期肿瘤患者, 营养治疗应遵循阶梯原则(A, 强推荐)。为保证充足能量, 非肥胖肿瘤患者推荐能量摄入量为 25 ~ 30 kcal / (kg· d),并根据患者个体情况(年龄、体力活动、应激系数等)进行适当调整(B, 强推荐)。
对于食欲下降的肿瘤患者, 蛋白质推荐摄入量为 1. 0 ~ 2. 0 g / (kg· d)(B, 强推荐)。对于食欲下降的肿瘤患者, 可适当提高脂肪供能比例,增加能量密度(C, 弱推荐)。
针对肿瘤患者厌食症状进行相应饮食调整, 有助于增强患者食欲, 增加营养摄入, 提高生活质量(B, 强推荐)。若患者经口摄入不足, 但消化道功能正常或具有部分消化道功能, 鼓励使用 ONS(A,强推荐)。富含免疫营养素的肠内营养制剂或 FSMP 或可帮助改善食欲, 保持或增加瘦体组织与体重( B, 弱推荐)。食欲下降的肿瘤患者应常规接受营养教育, 以维持健康饮食习惯和良好生活习惯(A,强推荐)。食欲下降的肿瘤患者, 应鼓励其通过运动来维持和改善食欲, 并根据健康状况和身体功能增减运动强度(A, 强推荐)。 执笔专家:张片红(浙江大学医学院附属第二医院) ;石汉平(首都医科大学附属北京世纪坛医院) ;陆彦妤(浙江大学医学院附属第二医院) ;张静芬(全国卫生产业企业管理协会医学营养产业分会)共识专家组成员(以姓氏笔画为序):于 康(中国医学科学院北京协和医学院北京协和医院) ;于吉人(浙江大学医学院附属第一医院) ;计云珍(嘉兴学院附属第二医院) ;石汉平(首都医科大学附属北京世纪坛医院) ;叶 孟(宁波大学医学院附属医院);史琳娜(南方医科大学南方医院) ;冯 霁(南昌大学第二附属医院) ;孙建琴(复旦大学附属华东医院) ;孙 新(吉林省人民医院);严森祥(浙江大学医学院附属第一医院);杨红琪(湖州市中心医院) ;应杰儿(浙江省肿瘤医院) ;沈 贤(温州医科大学附属第一医院) ;张片红(浙江大学医学院附属第二医院) ;张静芬(全国卫生产业企业管理协会医学营养产业分会) ;陆彦妤(浙江大学医学院附属第二医院);陈 伟(中国医学科学院北京协和医学院北京协和医院);陈立勇(山东大学附属省立医院) ;陈改云(郑州大学第一附属医院);陈秋霞(衢州市柯城区人民医院) ;陈洁文(上海交通大学附属第九人民医院);周 岚(昆明医科大学第三附属医院) ;周 莉(苏州大学附属第一医院) ;郑锦锋(中国人民解放军东部战区总医院) ;胡桂芬(浙江大学医学院附属金华医院);胡智明(浙江省立同德医院) ;姚 颖(华中科技大学同济医学院附属同济医院) ;黄晓旭(浙江大学医学院附属第二医院) ;蔡 斌(浙江大学医学院附属邵逸夫医院) ;潘宏铭(浙江大学医学院附属邵逸夫医院) ;戴福仁(温州医科大学附属第三医院)
- 三项特医食品特定全营养配方... 2026-05-20
- 近日,国家卫生健康委员会正式发布三项特殊医学用途配方食品特定全营养配方食品安全国家标准征求意见稿,涉及糖尿病全营养配方食品、肥胖症及...【详细】

